乳腺组织中的微小钙质沉积在影像检查中常呈现为“小白点”,这些看似寻常的发现可能让许多女性陷入焦虑。实际上,这种被称为“乳腺钙化”的现象既可能是生理性痕迹,也可能是疾病的信号,其背后隐藏着复杂的医学逻辑。
一、乳腺钙化的本质与分类

乳腺钙化是钙盐在组织中的异常沉积,通过乳腺X线(钼靶)检查可清晰识别为高密度亮点。根据临床意义,可分为两类:
1. 良性钙化:通常由乳汁残留、炎症修复、脂肪坏死或良性肿瘤(如纤维腺瘤)引发,形态多呈粗大颗粒状、环形或散在分布,例如“爆米花样”钙化是纤维腺瘤的典型表现。
2. 恶性钙化:多与乳腺癌相关,尤其是导管原位癌。这类钙化常呈现为密集的泥沙样、针尖状或分枝状,直径多小于0.5毫米,且在单位面积内成簇分布。
值得注意的是,钙化本身不会引发疼痛或肿块,其临床价值在于作为疾病诊断的“间接证据”。例如,约30%的乳腺癌早期仅通过钙化特征被发现。
二、钙化形成的机制探秘
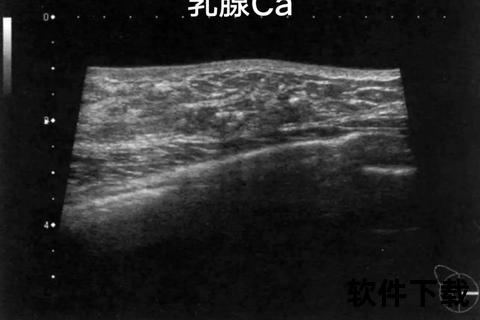
钙化的产生与局部代谢异常密切相关,目前主流理论认为:
环境因素也起辅助作用:长期高脂饮食可能增加乳腺组织炎症风险,间接促进钙化;而肥胖导致的雌激素水平升高,则与乳腺癌相关的恶性钙化有关。
三、诊断:影像技术揭示的微观世界
1. 钼靶X线摄影
作为黄金标准,钼靶能检测到0.2毫米的钙化点。医生通过分析钙化的形态、密度、分布进行分级:
典型案例:一名45岁女性钼靶显示右乳外上象限3处分枝状钙化(BI-RADS 4C),穿刺证实为导管原位癌。
2. 超声与MRI的辅助角色
高频超声可识别≥0.5毫米的钙化,尤其适合致密型乳腺;MRI则通过增强扫描评估钙化周围的血供情况,辅助判断恶性风险。
3. 病理活检的终极判断
对于可疑钙化,立体定位穿刺或导丝标记切除活检能明确性质。新技术如术中X线组织成像,可确保钙化灶被完整切除。
四、治疗策略:从观察到手术
良性钙化:
恶性钙化:
特殊案例:一名38岁女性钼靶发现左乳成簇微钙化(BI-RADS 4B),导丝定位切除后病理为良性腺病,避免过度治疗。
五、预防与管理:超越医学检查
值得关注的是,哺乳满12个月可使乳腺癌风险降低4.3%,这可能与哺乳期乳腺细胞分化成熟度提高有关。
行动建议:理性应对三步走
1. 报告解读:发现钙化时,关注BI-RADS分级而非钙化数量。例如“散在点状钙化(BI-RADS 2)”无需干预
2. 就医时机:若报告提示“形态不规则”“成簇分布”或分级≥4A,需在1周内就诊乳腺专科
3. 技术选择:优先选择配备数字化钼靶和超声弹性成像的医疗机构,诊断准确率可提升20%
一位52岁患者的经历具有借鉴意义:体检发现左乳钙化(BI-RADS 4A),经真空辅助活检确诊为良性导管扩张,通过定期随访避免不必要的手术。
乳腺钙化如同身体发出的加密信号,需要专业“解码”。通过科学认知与规范管理,既能避免过度焦虑,又能抓住早期治疗的黄金时机。正如医学界共识:不是所有钙化都指向癌症,但每一次异常发现都值得被认真对待。